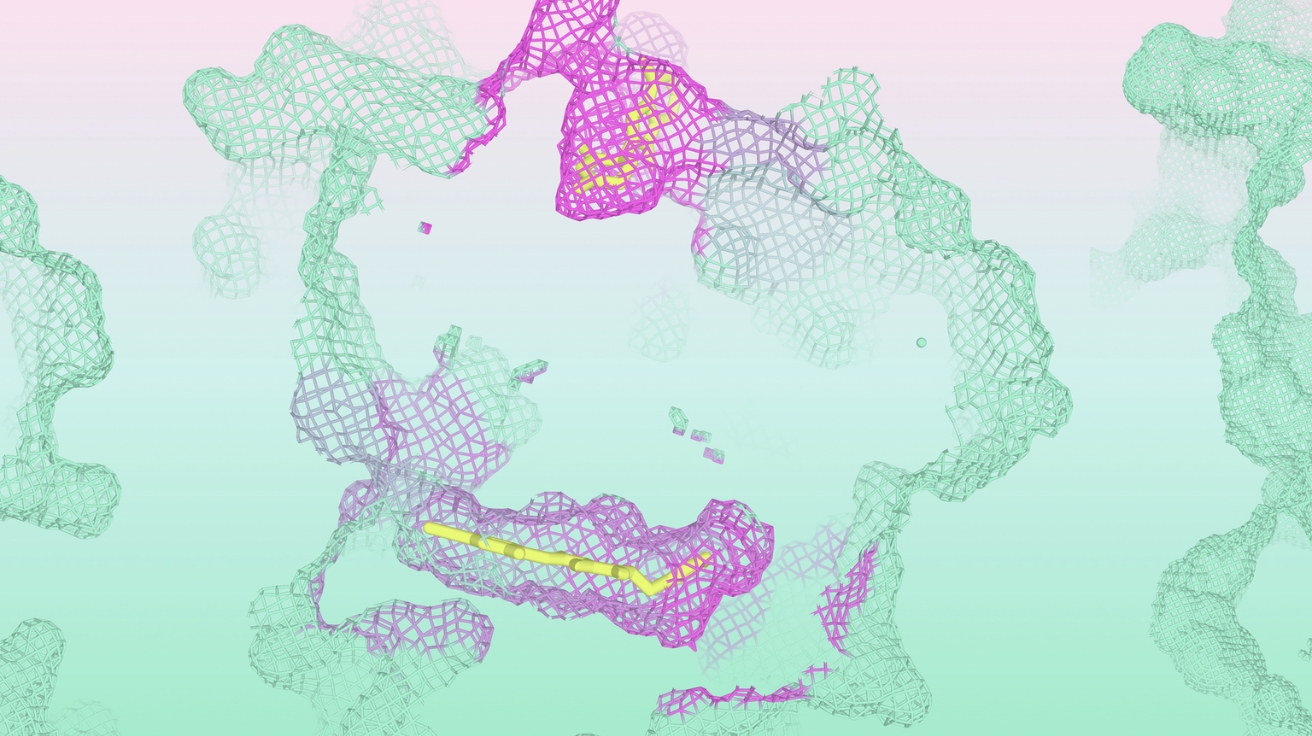
구글 딥마인드 계열사인 AI 신약 개발 기업 아이소모픽랩스(Isomorphic Labs)가 알파폴드3(AlphaFold 3)를 뛰어넘는 새로운 AI 신약 설계 시스템을 공개했다. 해당 리포트에 따르면, 이번에 발표된 아이소모픽랩스 신약 설계 엔진(IsoDDE)은 단백질 구조 예측 정확도를 2배 이상 높이고, 컴퓨터만으로 신약을 설계할 수 있는 능력을 대폭 강화했다고 밝혔다. 이는 실험실에서 수개월씩 걸리던 작업을 몇 초 만에 해낼 수 있다는 의미로, 신약 개발 과정의 혁신적 변화를 예고한다.
알파폴드3보다 2배 정확한 구조 예측… 미지의 영역까지 정복
아이소모픽랩스는 IsoDDE가 알파폴드3가 학습하지 않은 완전히 새로운 유형의 단백질-약물 결합 구조를 예측하는 데 있어 정확도를 2배 이상 높였다고 밝혔다. 특히 ‘Runs N’ Poses’ 벤치마크 테스트에서 가장 어려운 카테고리의 문제를 풀 때 이 같은 성과를 냈다. 이 테스트는 AI 모델이 한 번도 본 적 없는 새로운 형태의 단백질 주머니와 약물 분자를 얼마나 잘 예측하는지 측정한다.
더 주목할 점은 IsoDDE가 ‘유도 적합(induced fit)’과 ‘숨겨진 주머니(cryptic pocket)’ 같은 복잡한 생물학적 현상을 정확히 모델링할 수 있다는 것이다. 유도 적합이란 단백질이 약물 분자와 결합하기 위해 자신의 모양을 변형시키는 현상을 말하고, 숨겨진 주머니는 약물이 결합하기 전에는 보이지 않다가 결합 과정에서 드러나는 단백질 부위를 뜻한다. 이런 현상들은 신약 개발에서 매우 중요하지만 예측하기 극도로 어려운 영역이었다.
실제 사례로 IsoDDE는 NKG2D 단백질의 숨겨진 주머니에 결합하는 억제제의 구조를 성공적으로 예측했는데, 알파폴드3는 이 문제를 풀지 못했다. 이는 IsoDDE가 기존 AI 모델이 접근하지 못했던 미지의 생물학적 영역까지 정복할 수 있음을 보여준다.
항체 치료제 설계 능력 20배 향상… 복잡한 생물학적 치료제 시대 연다
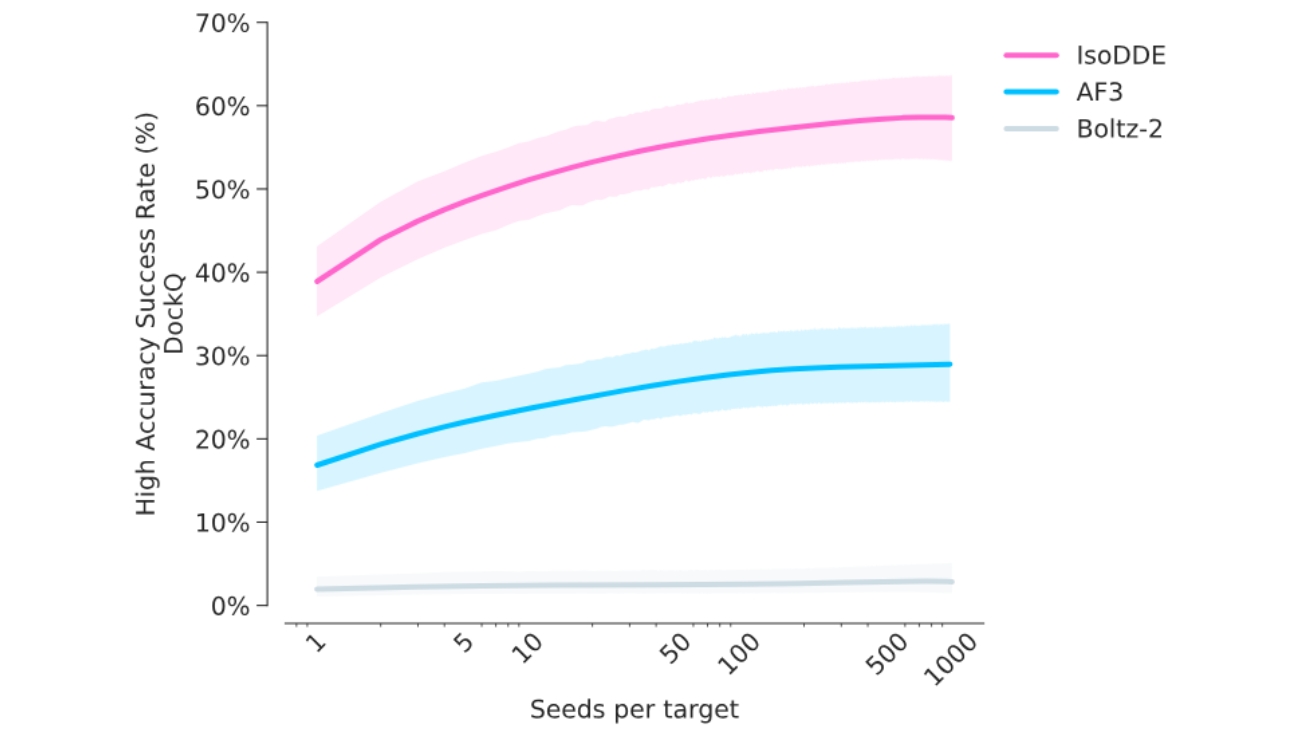
아스피린 같은 작은 분자 약물을 넘어 인슐린 같은 복잡한 생물학적 치료제 개발에서도 IsoDDE는 획기적인 성과를 냈다. 항체-항원 결합 구조를 예측하는 능력에서 알파폴드3보다 2.3배, 경쟁 모델인 볼츠-2(Boltz-2)보다는 무려 19.8배 높은 정확도를 보였다.
특히 항체에서 가장 변화무쌍하고 예측하기 어려운 부분인 CDR-H3 루프 구조를 정확히 예측할 수 있게 되면서, 완전히 새로운 항체 치료제를 컴퓨터상에서 설계할 수 있는 길이 열렸다. 항체 치료제는 암, 자가면역질환 등 다양한 난치병 치료에 사용되는데, 기존에는 개발 과정이 복잡하고 시간이 오래 걸렸다. IsoDDE는 이 과정을 대폭 단축시킬 수 있는 가능성을 제시한다.
이 성과는 334개의 까다로운 항체-항원 테스트 세트에서 검증됐으며, 고품질 예측(DockQ 점수 0.8 이상)을 달성한 비율에서 압도적인 우위를 보였다.
약물 결합력 예측에서 기존 물리 기반 방법 추월… 비용과 시간은 수천분의 일로
약물이 표적 단백질에 얼마나 강하게 결합하는지 예측하는 것은 효과적인 신약 개발의 핵심이다. 기존에는 FEP(자유 에너지 섭동법) 같은 물리 기반 계산 방법이 가장 정확했지만, 엄청난 계산 비용과 시간이 필요했고 실험으로 얻은 결정 구조가 반드시 필요했다.
IsoDDE는 FEP+ 4, OpenFE, CASP16 등 세 가지 공개 벤치마크에서 모든 딥러닝 기반 방법들을 큰 격차로 앞질렀다. 놀랍게도 실험 결정 구조 없이도 물리 기반 방법인 FEP를 능가하는 성능을 보였다. 이는 연구자들이 신약 개발 과정에서 수많은 후보 물질들을 빠르게 순위 매기고 최적화할 수 있음을 의미한다.
예를 들어 기존에는 약물 후보 물질 하나의 결합력을 정확히 계산하는 데 수일에서 수주가 걸렸다면, IsoDDE는 같은 작업을 몇 초 만에 해낼 수 있다. 이는 신약 개발 속도를 획기적으로 높이고 비용을 대폭 절감할 수 있는 가능성을 열어준다.
단백질 서열만으로 숨겨진 약물 결합 부위 찾아낸다… 15년 만의 발견을 재현
IsoDDE의 또 다른 혁신적 능력은 약물 없이도 단백질의 숨겨진 약점을 찾아낼 수 있다는 점이다. 마치 자물쇠의 열쇠 구멍을 찾는 것처럼, 단백질 어디에 약물이 들어갈 수 있는 구멍이 있는지 스스로 찾아낸다. 이는 완전히 새로운 방식의 신약을 개발하거나, 이미 잘 알려진 단백질이라도 지금까지와는 전혀 다른 방법으로 치료제를 만들 수 있다는 의미다.
대표적 사례가 세레브론(cereblon)이라는 단백질이다. 세레브론은 우리 몸에서 망가진 단백질을 제거하는 청소부 역할을 한다. 지난 15년간 과학자들은 이 단백질에 약물이 달라붙을 수 있는 곳이 딱 한 군데뿐이라고 생각했다. 탈리도마이드라는 약물이 결합하는 그 자리였다. 그런데 올해 초 연구진이 실험을 통해 완전히 새로운 결합 부위를 발견했다. 15년 만에 찾아낸 두 번째 열쇠 구멍이었다.
놀라운 점은 IsoDDE가 이 발견을 재현했다는 것이다. IsoDDE에게 세레브론 단백질의 설계도(아미노산 서열)만 보여줬더니, 어떤 약물 정보도 주지 않았는데 기존에 알려진 부위와 새로 발견된 숨겨진 부위를 모두 정확히 찾아냈다. 게다가 약물 분자를 알려주자, 각 약물을 올바른 위치에 정확히 배치했다. 실험실에서 수개월 걸리고 큰 비용이 드는 작업을 단 몇 초 만에 컴퓨터로 해낸 것이다.
이 기술은 지금까지 ‘약물을 만들 수 없는 단백질’로 여겨졌던 것들에 대해서도 새로운 가능성을 연다. 단백질의 숨겨진 약점만 찾아낼 수 있다면, 난치병 치료의 새로운 돌파구가 될 수 있기 때문이다.
FAQ (※ 이 FAQ는 본지가 리포트를 참고해 자체 작성한 내용입니다.)
Q1. IsoDDE가 알파폴드3보다 얼마나 더 정확한가요?
A. IsoDDE는 학습 데이터와 가장 다른 어려운 구조 예측 문제에서 알파폴드3보다 2배 이상 높은 정확도를 보입니다. 항체-항원 결합 예측에서는 알파폴드3보다 2.3배, 다른 경쟁 모델보다 최대 19.8배 더 정확합니다.
Q2. 이 기술이 실제 신약 개발에 어떻게 도움이 되나요?
A. IsoDDE는 실험실에서 수개월 걸리던 단백질 구조 분석과 약물 결합력 측정을 몇 초 만에 컴퓨터로 해결할 수 있습니다. 이를 통해 신약 개발 시간과 비용을 대폭 줄이고, 기존에는 불가능했던 새로운 타입의 치료제 설계가 가능해집니다.
Q3. 숨겨진 주머니(cryptic pocket)란 무엇이고 왜 중요한가요?
A. 숨겨진 주머니는 약물이 없을 때는 보이지 않다가 약물과 결합할 때만 나타나는 단백질의 결합 부위입니다. 이를 찾아내면 기존에 약물을 만들 수 없다고 여겨진 단백질에 대해서도 새로운 치료 방법을 개발할 수 있어 난치병 치료의 새로운 가능성을 열어줍니다.
기사에 인용된 리포트 원문은 아이소모픽랩스에서 확인 가능하다.
리포트명: The Isomorphic Labs Drug Design Engine unlocks a new frontier beyond AlphaFold
이미지 출처: 아이소모픽랩스
해당 기사는 챗GPT와 클로드를 활용해 작성되었습니다.